L'argon è il gas inerte più comunemente usato in glovebox e linee Schlenk per esperimenti altamente sensibili. Sebbene l'azoto sia un'alternativa meno costosa e più frequente, l'argon è strettamente preferito quando esiste il rischio che il gas "inerte" reagisca con i materiali sperimentali, cosa che può accadere con alcuni metalli o ad alte temperature.
La scelta tra argon e azoto è una decisione critica nella chimica sensibile all'aria, bilanciando il costo con la purezza chimica. Mentre l'azoto è un cavallo di battaglia economico, l'argon fornisce un livello superiore di inerzia, agendo come assicurazione essenziale per esperimenti altamente reattivi o ad alta temperatura.

Lo scopo di un'atmosfera inerte
La funzione principale di una glovebox o di una linea Schlenk è creare un ambiente controllato privo di componenti atmosferici reattivi. I principali colpevoli che si sta cercando di escludere sono l'ossigeno (O₂) e il vapore acqueo (H₂O), che possono facilmente decomporre reagenti e catalizzatori sensibili.
Un gas inerte, come argon o azoto, viene utilizzato per spostare l'aria e mantenere una pressione positiva, impedendo qualsiasi perdita atmosferica nel sistema.
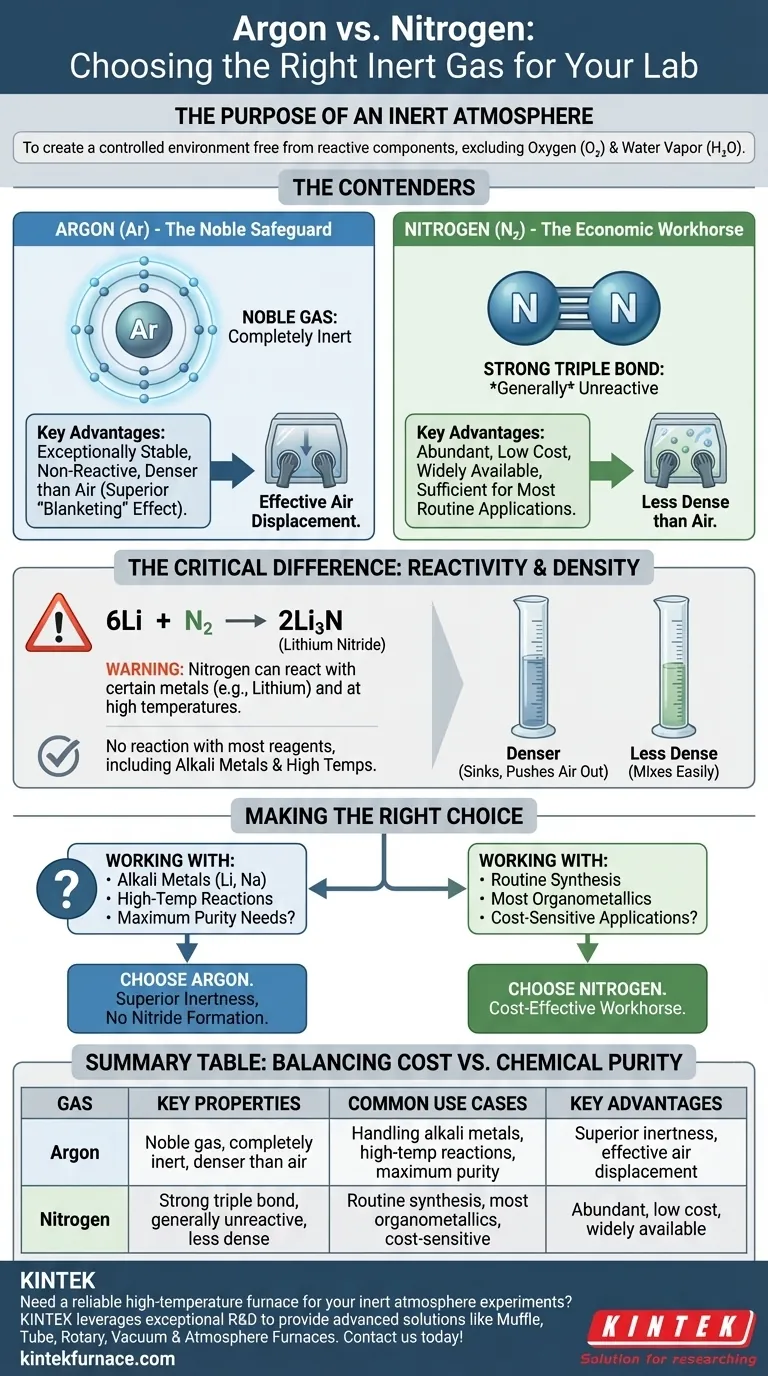
Confronto tra i contendenti: Argon vs. Azoto
Sebbene entrambi siano usati per creare un'atmosfera inerte, le loro proprietà chimiche e fisiche dettano quando uno è una scelta migliore dell'altro.
Azoto: Il cavallo di battaglia economico
L'azoto (N₂) costituisce circa il 78% dell'aria che respiriamo ed è quindi abbondante e poco costoso.
La molecola di N₂ è caratterizzata da un legame triplo molto forte tra i suoi due atomi di azoto. Questo legame richiede una notevole quantità di energia per essere rotto, motivo per cui l'azoto è generalmente non reattivo e adatto a un'ampia gamma di applicazioni chimiche.
Argon: La salvaguardia nobile
L'argon (Ar) è un gas nobile. Ciò significa che i suoi atomi hanno un guscio elettronico esterno completamente riempito, rendendolo eccezionalmente stabile e non reattivo.
In praticamente tutte le condizioni di laboratorio, l'argon non formerà legami chimici né reagirà con i reagenti. Questa fondamentale inerzia chimica è la sua più grande forza.
La differenza critica: Reattività
Il termine "inerte" è relativo. Sebbene l'azoto sia per lo più non reattivo, non è completamente inerte.
In condizioni specifiche, l'azoto può reagire con alcuni metalli per formare nitruri metallici. L'esempio più comune nella chimica sintetica riguarda il litio metallico, che reagisce prontamente con il gas N₂ anche a temperatura ambiente per formare nitruro di litio (Li₃N).
6Li + N₂ → 2Li₃N
Questa reazione secondaria indesiderata può consumare il reagente e introdurre impurità. Reazioni simili possono verificarsi con altri metalli alcalini, metalli alcalino-terrosi o durante sintesi condotte ad alte temperature. L'argon, come gas nobile, non ha questa responsabilità.
Una considerazione pratica: Densità del gas
Una differenza fisica chiave è la densità. L'argon è circa il 40% più denso dell'aria, mentre l'azoto è leggermente meno denso dell'aria.
Ciò significa che l'argon è più efficace nello spostare l'aria da un contenitore, poiché "affonderà" e spingerà l'aria più leggera verso l'alto e fuori. Questo effetto "coperta" lo rende superiore per la purga di vetreria su una linea Schlenk e per mantenere un'atmosfera stabile all'interno di una glovebox, poiché si deposita sul fondo piuttosto che mescolarsi facilmente.
Comprendere i compromessi
La scelta del gas giusto richiede un equilibrio tra sicurezza assoluta e vincoli pratici.
Costo: Il fattore trainante principale
Il vantaggio più significativo dell'azoto è il suo basso costo. L'argon è sostanzialmente più costoso dell'azoto.
Per i laboratori che gestiscono molte glovebox o eseguono sintesi su larga scala, questa differenza di costo può essere un fattore importante. Per questo motivo, l'azoto è spesso la scelta predefinita per qualsiasi lavoro in cui la sua potenziale reattività non è un problema.
Purezza e fornitura
Entrambi i gas sono disponibili in commercio in gradi di purezza molto elevata (ad esempio, 99,999%). La differenza chiave spesso risiede nel metodo di fornitura.
Gli utenti di azoto su larga scala possono disporre di generatori in loco o di grandi serbatoi di azoto liquido che forniscono un flusso continuo di gas per evaporazione, riducendo ulteriormente i costi operativi. L'argon viene quasi sempre fornito in bombole di gas ad alta pressione, che richiedono una sostituzione regolare.
Fare la scelta giusta per il tuo esperimento
La tua decisione dovrebbe basarsi sulla chimica specifica che stai eseguendo.
- Se il tuo obiettivo principale è la sintesi di routine, la purificazione o la manipolazione della maggior parte dei composti organometallici: Usa l'azoto. È sufficientemente inerte per la stragrande maggioranza delle applicazioni e offre notevoli risparmi sui costi.
- Se il tuo obiettivo principale è lavorare con litio, altri metalli alcalini o eseguire reazioni ad alta temperatura: Usa l'argon. La sua inerzia superiore non è negoziabile e protegge il tuo esperimento dalla formazione di nitruri metallici indesiderati.
- Se il tuo obiettivo principale è la massima certezza ed eliminare tutte le variabili: Usa l'argon. Il costo più elevato è un piccolo prezzo da pagare per la garanzia che il tuo gas inerte sia veramente inerte.
In definitiva, comprendere la sottile reattività dell'azoto è ciò che separa la pratica di routine dalla progettazione sperimentale precisa e deliberata.
Tabella riassuntiva:
| Gas | Proprietà chiave | Casi d'uso comuni | Vantaggi chiave |
|---|---|---|---|
| Argon | Gas nobile, completamente inerte, più denso dell'aria | Manipolazione di metalli alcalini, reazioni ad alta temperatura, esigenze di massima purezza | Inerzia superiore, efficace spostamento dell'aria, nessuna formazione di nitruri |
| Azoto | Legame triplo forte, generalmente non reattivo, meno denso dell'aria | Sintesi di routine, la maggior parte dei composti organometallici, applicazioni sensibili ai costi | Abbondante, basso costo, ampiamente disponibile |
Hai bisogno di un forno ad alta temperatura affidabile per i tuoi esperimenti in atmosfera inerte? KINTEK sfrutta un'eccezionale ricerca e sviluppo e la produzione interna per fornire soluzioni avanzate come forni a muffola, a tubo, rotativi, a vuoto e ad atmosfera, e sistemi CVD/PECVD. Con forti capacità di personalizzazione profonda, soddisfiamo precisamente le tue esigenze sperimentali uniche. Contattaci oggi per migliorare l'efficienza e la sicurezza del tuo laboratorio!
Guida Visiva
Prodotti correlati
- Forno tubolare al quarzo da laboratorio multizona Forno tubolare
- Forno a muffola ad alta temperatura per il laboratorio di deceraggio e pre-sinterizzazione
- Forno ad atmosfera controllata con nastro a rete Forno ad atmosfera inerte con azoto
- Forno a Muffola da 1200℃ per Laboratorio
- Forno a tubo rotante a più zone di riscaldamento Split Forno a tubo rotante
Domande frequenti
- Quali sono i vantaggi dei forni a tubo a zone multiple? Ottieni un controllo termico superiore per l'elaborazione di materiali avanzati
- Quale ruolo svolgono i forni a tubo multizona nella ricerca sulle nuove energie? Sblocca un controllo termico preciso per l'innovazione
- Quali applicazioni di protezione ambientale utilizzano forni a tubi multizona? Sblocca la precisione nel trattamento dei rifiuti e nella tecnologia verde
- Come funziona il sistema di controllo della temperatura in un forno a tubo sperimentale a gradienti multipli? Domina i profili termici precisi per il tuo laboratorio
- Perché i forni tubolari multizona sono particolarmente utili per la ricerca sui nanomateriali?Precisione ed efficienza per i materiali avanzati



















